类器官(organoid)研究专题
二十世纪六十年代到八十年代,3D培养已经成为生物学研究的热点,当时利用3D培养技术主要是在体外模拟组织器官生成的过程,将胚胎干细胞分化培养成微型器官,借以研究器官发育的发生机制。从2009年Clevers实验室第一次用成体干细胞,即小肠干细胞培育出具备小肠绒毛和隐窝结构的类器官以来,组织类器官培养再次成为明星技术,2013年和2017年分别被Science和Nature Methods杂志评为年度十大进展和突破。从实验动物到人样本,从组织干细胞分化培养到直接组织培养,从单一细胞结构到多种细胞基质的加入,组织类器官从发育生物学研究工具变成肿瘤研究的利器。

类器官是源于多能干细胞或器官祖细胞且具有胚层特异性的类器官体, 其包含目标器官中至少一种细胞类型, 能够自组装为器官样结构并具有其生理结构和功能特征。
类器官优势
l 与细胞系相比,具有组织结构和器官功能,能最大程度模拟人体器官;
l 取材广泛,采集胸腹水和穿刺活检组织也能完成,大部分人体组织器官能在体外培养成组织类器官,而且不存在伦理问题;
l 类器官体外培养成功率高,培养速度快,适合大规模扩增,长期培养仍能保持基因组稳定;
l 体外3D类器官能用于体内移植,有望解决器官修复再生问题;
l 肿瘤类器官用于指导临床用药,周期短、数据分析简单,重要的是类器官药物敏感性数据较测序结果更加准确;
l 与基因编辑技术结合,能够实现器官水平上的基因改造。
类器官培养
直接通过肿瘤组织培养或干细胞分化,辅以细胞因子、肿瘤基质等补充,是肿瘤类器官研究的发展趋势。
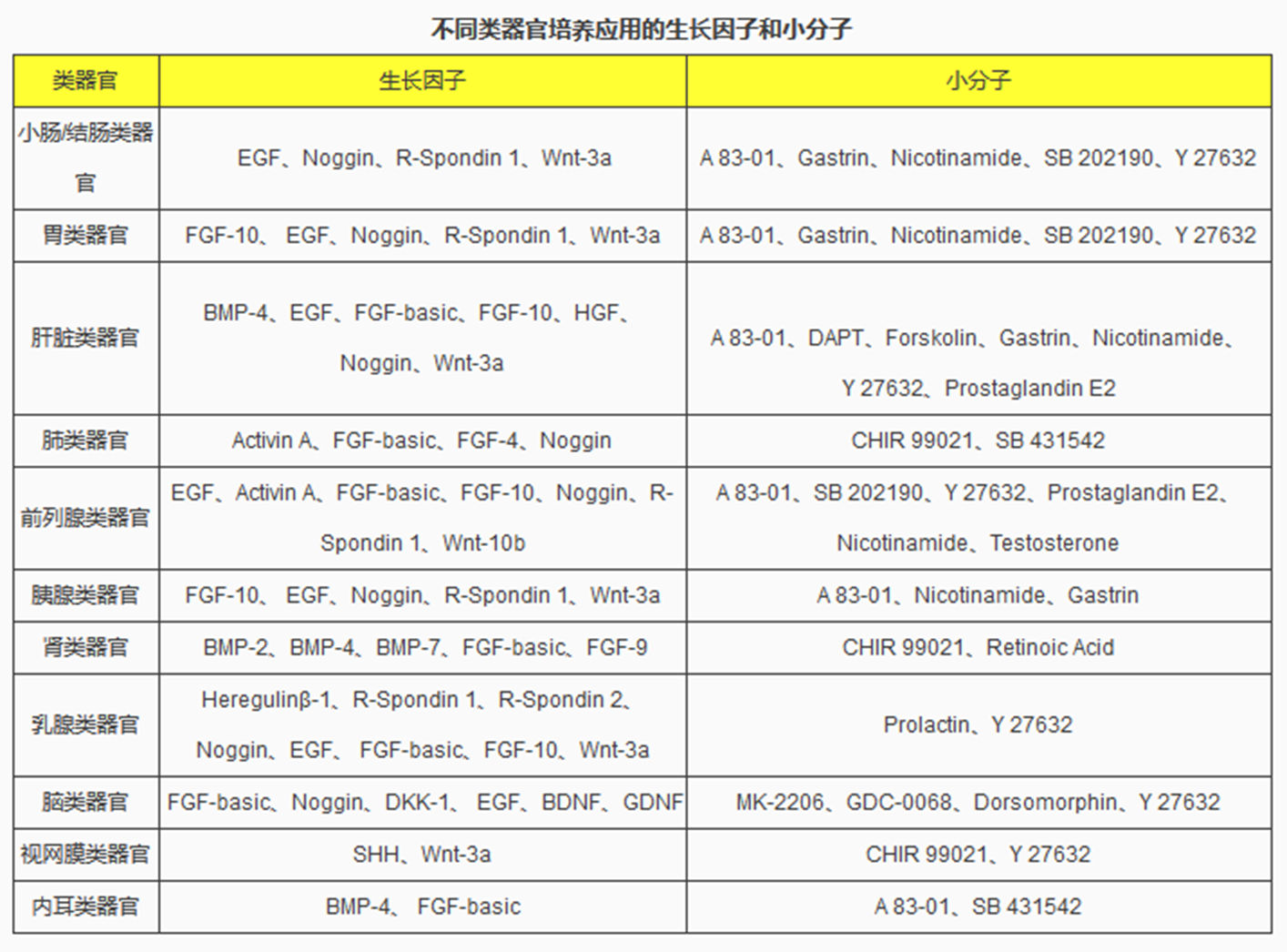
培养流程
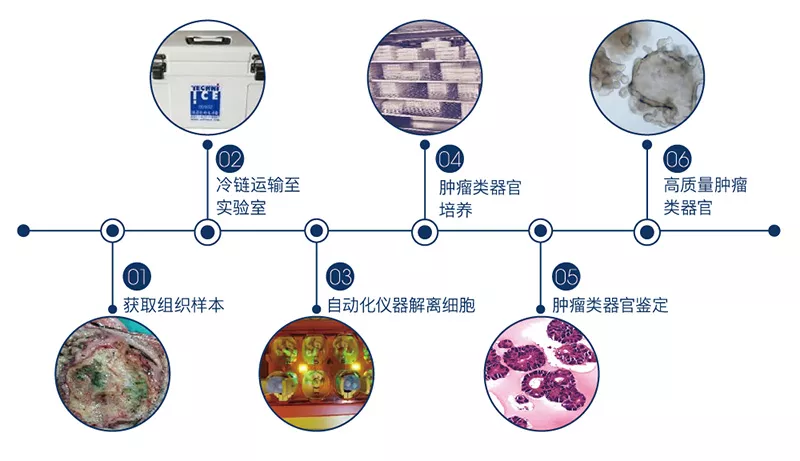
类器官应用方向
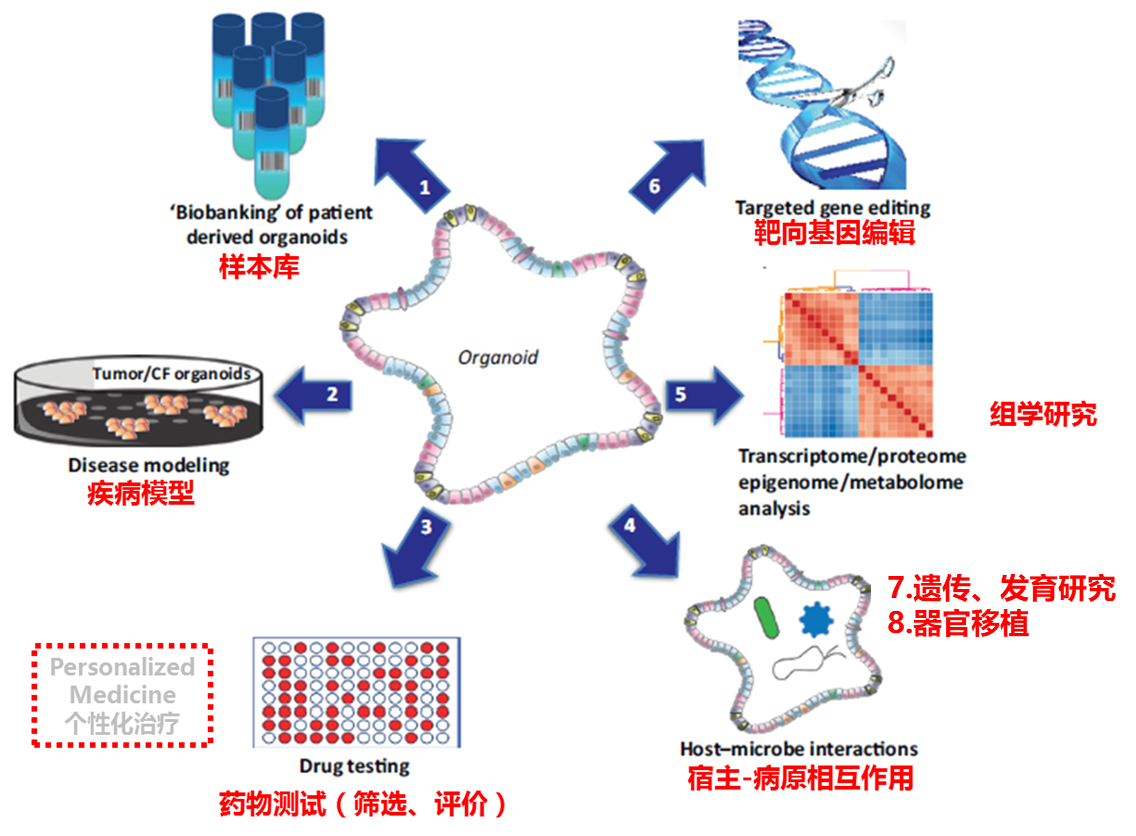
类器官服务范围
l 类器官培养(人/动物)与鉴定
l 类器官药物敏感性筛选
l 类器官免疫组化
l 类器官免疫荧光
l 类器官培养动态监测